
7月22日,由转化医学国家重大科技基础设施(上海)创新医疗器械注册研究与临床转化服务中心(NFTM-MRC)主办的上海交通大学长三角创新医疗器械注册研究与临床转化系列课程(YMRC)第9期在线上举行。出席课程的有NFTM-MRC主任、上海交通大学医学院附属第九人民医院王金武教授, 泰格捷通体外诊断部张勇琴总监、创新医疗器械注册研究与临床转化服务中心许苑晶等。论坛由张勇琴讲解《IVD产品上市前注册和临床流程概览》、许苑晶主持。课程由王金武主任致辞,他提到近年来随着体外诊断试剂迅速发展、医院的广泛应用,体外诊断试剂从设计开发、临床试验、生产制造、注册申报到临床使用面临诸多挑战,特邀泰格捷通体外诊断部总监张勇琴分享IVD产品上市前注册和临床试验经验。
许苑晶介绍NFTM-MRC的工作开展情况,中心由戴尅戎院士担任名誉主任,依托高校进行产学研医用相关标准、检测、注册研究一体的技术服务,并开展高校试制基地与监管科学的探索,旨在协助科研团队加速医疗器械产业化。

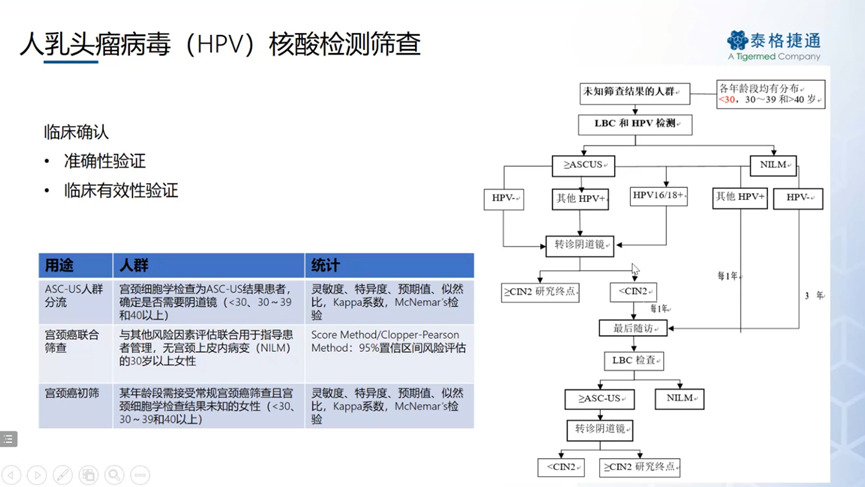
张勇琴总监从体外诊断试剂的全生命周期管理入手,介绍了国内注册管理法规、技术文件体系和监管部门,从质量管理体系角度介绍了产品实现过程,以及各阶段对应的工作内容、设计开发文档和注册申报资料之间的关联。同时她强调了设计变更和全生命周期的风险管理、前期设计输入的重要性,重点向与会人员介绍了体外诊断试剂注册申报流程、注册申报材料,创新、优先审批、应急医疗器械申报条件和法规依据临床评价路径,包括FDA、CE注册申报流程及相关要求等。最后,张勇琴总监以“人乳头瘤病毒(HPV)核酸检测筛查产品”为例,讲解了相关产品的临床试验设计,对与会者提出的肿瘤体外诊断试剂注册申请难点进行了热心解答。

上海交大创新医械注册转化服务中心将持续提供优质的线上课程,所有线上学员均可申请成为上海交大转化注册中心会员,成为上海交大注册转化Family的成员,免费获得今后学术通知与生物医药产业转化服务的机会!



Copyright © 2022 Corporation All Rights Reserved
地址:上海市闵行区剑川路上海交通大学闵行校区 邮编:201203
沪交ICP备20220211 技术支持:戴院士王金武教授科研团队